- HOME
- Enzyme List
- BPF-301・302 Blocking Peptide Fragment
BPF-301・302
Blocking Peptide Fragment from Microorganism
PREPARATION and SPECIFICATION
| Appearance | White amorphous powder, lyophilized | |
|---|---|---|
| Activity | GradeⅢ | |
| Contaminants | Inorganic phosphate | ≤ 0.01 mg/g |
| Alkaline phosphatase | ≤ 1×10-4 U/mg | |
PROPERTIES
| Stability | Stable at 4 ℃ for at least 6 months(Fig.4) |
|---|---|
| Molecular weight | approx. 22,000 (SDS-PAGE) |
APPLICATIONS
This peptide fragment is useful as a blocking reagent for ELISA, offering an alternative to BSA.
FEATURES
| 1. Efficiency | Excellent blocking performance.(Fig.1) |
|---|---|
| 2. Operation Tim | Shorter time of operation(Fig.2) |
| 3. Sensitivity | No interference on ELISA assay(Fig.3) |
Examples
-
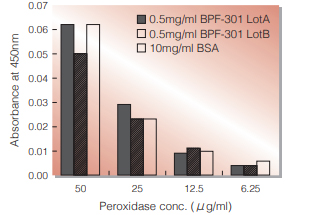
Fig.1. BPF-BSA Comparison: Blocking Efficiency
Peroxidase solutions containing BPF-301 or BSA were added to 96 wells polystyrene plate. The plate was incubated at 37 ℃ for 1hr and then washed with 0.02 % Tween20. The blocking performance was evaluated by measuring the peroxidase activities retained on polystyrene plate. The lower absorbance shows the higher blocking performance. Blocking performance of BPF-301 is much higher than that of BSA.
-
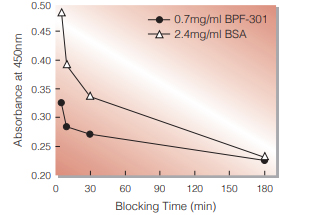
Fig.2. BPF-BSA Comparison: Blocking Time
BPF-301 or BSA solution was added to 96 wells polystyrene plate. The plate containing these blocking reagent was incubated at 4 ℃ for 5~180 minutes, and then washed with 0.02 % Tween20. The blocking performance was measured by human serum and anti-human IgG goat antibody POD conjugate system. Operation time required for blocking reaction is shorter than that of BSA.
-
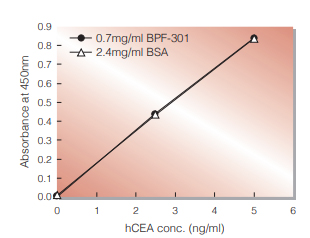
Fig.3. BPF-BSA Comparison: Measuring sensitivity
BPF-301 or BSA was used as a blocking reagent in ELISA assay for detection of hCEA. It was shown that no interference on ELISA assay was found in BPF-301.
-
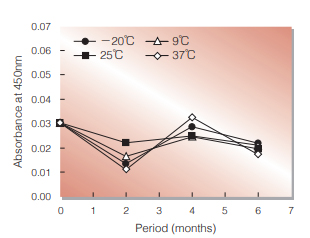
Fig.4. Stability (Powder form)
Blocking performance was measured by the method mentioned in Fig.1.
使用例(Japanese)
例-1:ブロッキング能の簡易測定法
1.試薬
- BPF溶液
5㎎のBPF-301をPBS 10 mLに溶解する。 - BSA溶液(対照実験用)
100㎎のBSAをPBS 10 mLに溶解する。 - POD溶液
2㎎のPeroxidase(TOYOBO PEO-131)を上記BPF溶液又はBSA溶液1 mLに溶解する。 - プレート洗浄液
0.02gのTween20を100 mLのPBSに溶解する。 - TMB溶液
BioRad TMB substrate Kit (Cat.No.:172-1067)
2.手順
1.BPF溶液(試薬A)又はBSA溶液(試薬B)により, POD溶液(試薬C)を希釈する。
2. 上記POD希釈液100μlを96穴ポリスチレンプレートに添加, 室温にて1時間インキュベートする。
3.プレート中の溶液を捨て,プレート洗浄液(試薬 D)によりプレートを洗浄する。
4.TMB溶液(試薬E)100μlを添加, 37℃にて10分間インキュベートし発色させる。
5.1N H2SO4 100μlの添加により反応を停止した後, 450nmにおける吸光度を測定する。吸光度が低いほどブロッキング能が高い。
3.結果
優れたブロッキング能が確認された。(Fig.1参照)
例-2:BPF-301とBSAの操作時間の比較
1.試薬
- BPF溶液
: 7㎎のBPF-301を10 mLの20mM Tris-HCl, pH7.0に溶解する。 - BSA溶液(対照実験用)
: 24㎎のBSAを10 mLの20mM Tris-HCl, pH7.0に 溶解する。 - ヒト血清希釈液
: PBSにてヒト血清を希釈する(50倍希釈)。 - プレート洗浄液
: 0.02gのTween20を100 mLのPBSに溶解する。 - TMB溶液
: BioRad TMB substrate Kit (Cat.No.:172-1067) - anti-human IgG goat antibody POD conjugate
2.手順
1.BPF溶液(試薬A)又はBSA溶液(試薬B)100μlを96穴ポリスチレンプレートに添加, 4℃にて数分~3時間インキュベートする。
2.プレート中の溶液を捨て,ヒト血清希釈液(試薬C) 25μlを添加する。
3.プレート中の溶液を捨て,プレート洗浄液(試薬D) によりプレートを洗浄する。
4.anti-human IgG goat antibody POD conjugate(試薬F)50μlを添加, 37℃にて1時間インキュベートする。
5.プレート中の溶液を捨て, プレート洗浄液(試薬D)によりプレートを洗浄する。
6.TMB溶液(試薬E)50μlを添加, 室温にて5分間インキュベートし発色させる。
7.1N H2SO4 50μlの添加により反応を停止した後, 450nmにおける吸光度を測定する。吸光度が低いほどブロッキング能が高い。
3.結果
BSAより短い操作時間で高いブロッキング能が得られた。操作時間は30分間で十分であった。(Fig.2 参照)
例-3:BPFとBSAの感度比較
1.試薬
- BPF溶液
: 7mgのBPF-301を10 mLの20mM Tris-HCl, pH7.0に溶解する。 - BSA溶液(対照実験用)
: 24mgのBSAを10 mLの20mM Tris-HCl, pH7.0に溶解する。 - プレート洗浄液
: 0.02gのTween20を100 mLのPBSに溶解する。 - TMB溶液
: BioRad TMB substrate Kit (Cat.No.:172-1067) - hCEA MoAb溶液
: carbonate buffer, pH9.6にてhCEAを希釈する (10ug/mL)。 - CEA MoAb-POD conjugate
: carbonate buffer, pH9.6にてCEA MoAb-POD conjugateを希釈する(250倍希釈)。 - hCEA 標準液
2.手順
1.hCEA MoAb(試薬E)100μlを96穴ポリスチレンプレートに添加, 37℃にて1時間インキュベートする。
2.BPF溶液(試薬A)又はBSA溶液(試薬B)100μlを添加, 4℃にて3時間インキュベートする。
3.プレート中の溶液を捨て, hCEA 標準液(試薬G)50μl を添加, 37℃にて1時間インキュベートする。
4.プレート中の溶液を捨て, プレート洗浄液(試薬C)にてプレートを洗浄する。
5.CEA MoAb-POD conjugate(試薬F)50μlを添加, 37℃にて1時間インキュベートする。
6.プレート中の溶液を捨て, プレート洗浄液(試薬C)にてプレートを洗浄する。
7.TMB溶液(試薬D)50μlを添加, 室温にて5分間インキュベートし発色させる。
8.1N H2SO4 50μlの添加により反応を停止した後, 450nmにおける吸光度を測定する。吸光度が低いほどブロッキング能が高い。
3.結果
ELISAアッセイへの阻害は全く検出されなかった。 (Fig.3参照)
CONTACT
-
For inquiries and cosultations regarding our products, please contact us through this number.
- HEAD OFFICE+81-6-6348-3843
- Inquiry / Opinion
